Covid-19: un complicato processo per l’ottenimento di un vaccino efficace
- martaluc95
- May 30, 2020
- 7 min read
Click here for the English version 🇬🇧
“È una gara contro la scomparsa del virus, e contro il tempo”
Queste le parole rilasciate dal Professor Adrian Hill, direttore dell’istituto universitario Jenner Institute al Telegraph in un’intervista esclusiva del 23 maggio scorso. Il Professor Hill sta guidando lo sviluppo del potenziale vaccino ChAdOx1 nCoV-19, conosciuto anche come AZD1222, insieme all’Oxford Vaccine Group dell’Università di Oxford. Questo vaccino è stato ottenuto attraverso la modificazione genetica di un virus che causa infezioni negli chimpanzee, in modo da indebolirlo e impedirne la replicazione nel corpo umano. Successivamente, sono state eseguite altre modificazioni per rendere il materiale genetico capace di produrre una proteina tipica del virus Covid-19, detta proteina Spike, presente sulla superficie del virus e che gli permette di entrare nelle cellule umane. Al momento dell’esposizione al virus, AZD1222 dovrebbe indurre il sistema immunitario umano a riconoscerne la proteina Spike e attivare una risposta difensiva che interrompe l’ingresso del patogeno nelle cellule umane e quindi prevenire l’infezione.
Lo scorso aprile il gruppo di ricerca di Oxford ha stimato intorno all’80% la probabilità di successo del vaccino, e la capacità di distribuirne un milione di dosi già da settembre 2020, una volta terminati i test e anticipando di molto quei 12-18 mesi necessari per ottenerlo secondo la maggioranza degli esperti di tutto il mondo. Tuttavia, la continua decrescita del numero di persone infette in Inghilterra crea negli scienziati il timore che esso possa scomparire. I ricercatori di Oxford, per poter verificare l’efficacia del vaccino, necessitano di centinaia di persone colpite dal Covid-19 per poter confrontare il numero degli infetti del gruppo di controllo col numero di infetti del gruppo di persone vaccinate.
AZD1222 ha già superato la Fase 1 degli studi clinici che ha coinvolto circa 1100 persone (volontari sani di età compresa tra i 18 e i 55 anni) in un studio cieco necessario a testare il profilo di sicurezza del vaccino (ovvero per verificare che esso non induca reazioni avverse) e la sua capacità di indurre una risposta immunitaria. I volontari coinvolti nello studio sono stati divisi in maniera random tra due gruppi: al primo gruppo è stato somministrato il vaccino AZD1222, mentre ai volontari del secondo gruppo è stato somministrato un vaccino già in uso contro il meningococco. La somministrazione di quest’ultimo solo ad alcuni soggetti è stata funzionale alla costituzione di un gruppo di “controllo” per confrontare gli eventuali effetti collaterali e le risposte immunitarie indotte dai due vaccini. È ovvio che per misurare gli effetti positivi e negativi di un vaccino sull’uomo, il confronto non può essere fatto con la somministrazione di una semplice soluzione salina al gruppo di “controllo”, per due ragioni. Innanzitutto, questa non potrebbe indurre neanche i più lievi effetti collaterali di un vaccino (per esempio dolore al braccio, malditesta e febbre). Inoltre, i volontari appartenenti al gruppo di controllo intuirebbero l’identità della soluzione assunta, rischiando di influenzare il loro comportamento durante lo studio clinico. È per questo quindi che lo studio è detto “cieco”, poichè nessuno dei partecipanti sa a quale gruppo appartiene e le loro risposte al test non vengono influenzate da preconcetti. I dati ottenuti sul profilo di sicurezza di AZD1222 sono risultati positivi: infatti, i volontari trattati con AZD1222 non hanno presentato effetti collaterali gravi, ma solo febbre leggera, malditesta e indolenzimento all’arto.
Tuttavia, prima di inizare i test sull’uomo, i ricercatori di Oxford avevano testato il potenziale vaccino sugli animali, su cui non ebbe livelli di efficacia soddisfacenti nell’attivare una risposta immunitaria nell’organismo – ovvero non è riuscito a proteggerli dall’infezione. In questo caso, delle scimmie erano state tutte volontariamente esposte al SARS-CoV-2 e poi divise in due gruppi, di cui solo uno venne vaccinato con una singola dose di AZD1222. Lo studio ha dimostrato che nel gruppo di scimmie vaccinate il virus non è riuscito a raggiungere i polmoni – anche se nel loro naso venne trovata una quantità di virus paragonabile a quella presente nel naso delle scimmie non vaccinate. Ciò significa che il vaccino ha prevenuto l’insorgenza della polmonite (la peggiore complicazione che il virus può indurre nell’uomo), ma non ha protetto gli animali dall’infezione nè dalla sua possibile trasmissione. Questi risultati potrebbero essere giustificati dal fatto che la dose di vaccino somministrata alle scimmie fosse insufficiente rispetto all’alta dose di virus a cui le stesse erano state esposte. Se così fosse, una seconda iniezione del vaccino potrebbe aumentare apprezzabilmente la risposta immunitaria. Questi test sugli animali sono in ogni caso essenziali per sviluppare previsioni sui risultati dei test sull’uomo.
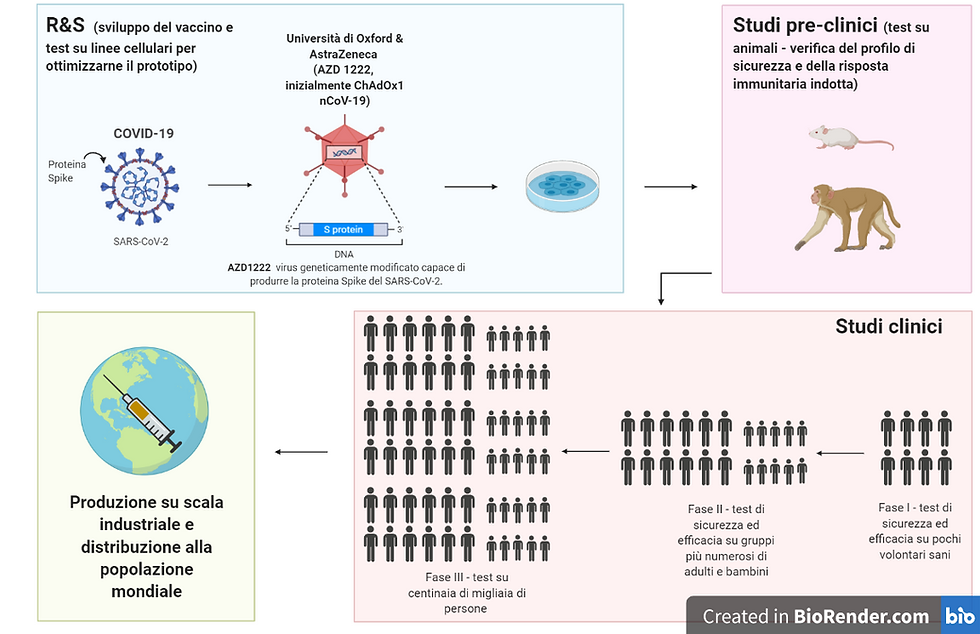
Una volta osservato che lo stato di salute delle scimmie non era stato compromesso, l’Oxford Vaccine Group ha iniziato a reclutare un numero 10 volte maggiore di persone per svolgere gli studi clinici di Fase 2/3 per verificare gli effetti del vaccino su una popolazione adulta e pediatrica e determinare se esso operi efficacemente nel prevenire l’infezione, ma anche per osservare l’eventuale sviluppo di compromissioni dovute all’infezione negli stessi soggetti. Se il vaccino si rivelerà efficace, la sua somministrazione alla popolazione generale verrà immediatamente approvata per “uso emergenziale”. Questa sarebbe davvero un’ottima prospettiva e per essere raggiunta è necessario che la diffusione del virus non si azzeri troppo velocemente. “La velocità con cui riusciremo a raccogliere il numero [di dati] necessari dipenderà dal livello di trasmissione del virus nella popolazione. Se la velocità di trasmissione rimarrà alta, potremmo ottenere i dati [di efficacia] del vaccino in un paio di mesi, ma se il livello di trasmissione crolla, potrebbero volerci più di 6 mesi” ha dichiarato il Professor Hill.
Chi sta sostenendo lo sviluppo di AZD1222? Dopo aver ricevuto 20 millioni di sterline dal governo inglese, il Jenner Institute e l’Oxford Vaccine Group alla fine di aprile hanno annunciato un accordo con la compagnia bio-farmaceutica AstraZeneca, che ha sede legale a Cambridge, la quale è divenuta responsabile per lo sviluppo, la produzione e la distribuzione del vaccino a livello mondiale. Infatti, intanto che venivano organizzati e condotti i primi studi clinici, la produzione del vaccino è stata convertita su scala industriale per rispondere alla grande quantità di dosi necessarie a svolgere gli studi clinici più avanzati e, potenzialmente, per un successivo uso a livello planetario. Il metodo di produzione iniziale è stato sviluppato a Oxford sotto la guida del Dr. Alexander Douglas, ma necessita di un importante processo di scale-up. AstraZeneca ha assicurato la totale capacità produttiva di ben un milione di dosi, che inizierà a distribuire già da settembre 2020, prima ai cittadini britannici e poi al resto del mondo. Contemporaneamente sono state avviate diverse filiere produttive che operano in parallelo per garantire ampio accesso al vaccino e un processo di produzione che non alteri la qualità del prodotto biotecnologico. Il 21 maggio scorso l’AstraZeneca ha ricevuto più di 1 miliardo di dollari dall’autorità americana Biomedical Advanced Research and Development Authority (BARDA) per sostenere lo sviluppo, la produzione e la distribuzione di AZD1222. Un gruppo di esperti della BARDA si sta impegnando eccezionalmente a produrre migliaia di dosi del vaccino, rappresentando essa stessa una catena produttiva che opera in parallelo con lo speciale obiettivo di ottimizzare la qualità del processo. BARDA sta anche finanziando e monitorando molti altri progetti di sviluppo in tutto il mondo per la lotta contro il Covid-19 (come per esempio lo sviluppo dei vaccini di Moderna e Janssen - entrambi hanno riportato risultati positivi negli studi clinici di Fase 1). Un’altra filiera che opera in parallelo all’AstraZeneca è attiva presso la IRBM, azienda con sede a Pomezia, che ha fornito centinaia di dosi del vaccino all’Università di Oxford per condurre i suoi test.
È evidente che si sta sostenendo un enorme sforzo internazionale per supportare il progresso scientifico a favore della salute pubblica. La discussione internazionale si è spostata anche sul welfare globale: sul piatto ci sono ingenti interessi economici che fanno salire la preoccupazione per un paritario accesso mondiale al vaccino. AstraZeneca si sta accordando con diverse organizzazioni internazionali come la Coalition for Epidemic Preparedness Innovations (CEPI), Gavi the Vaccine Alliance e la World Health Organisation (WHO) per un’equa distribuzione del vaccino in tutto il pianeta e sta dirigendo tavoli di discussione coi governi mondiali per aumentare l’accesso al trattamento. Inoltre, sta instaurando collaborazioni con partner asiatici come il Serum Institute of India ed altri per lanciare anche nei Paesi emergenti la produzione e la distribuzione di AZD1222.
La partecipazione di investitori privati è essenziale per il successo del progetto. Tra i co-fondatori della CEPI ci sono i leaders della Bill & Melinda Gates Foundation e nel 2011 la coppia di miliardari ha dato il via alla “Decade dei vaccini” insieme alla WHO per finanziare e dirigere la scoperta di nuovi vaccini contro le future pandemie.
La WHO sta svolgendo un serrato lavoro di coordinazione internazionale: l’organizzazione ha stabilito specifiche linee guida sullo sviluppo del vaccino che i vari centri di ricerca devono rispettare per ottenere una collaborazione reciproca. A gennaio la WHO ha pubblicato i primi criteri sul meccanismo d’azione del vaccino sostenuti da scienziati esperti, dichiarando che: “I partecipanti hanno enfatizzato l’importanza che il meccanismo antigenico mediato dal vaccino veda preferibilmente come target la proteina nCoV Spike” (così come inizialmente abbiamo detto opera il vaccino di Oxford). Ad aprile la WHO ha esposto alle compagnie private e alle istituzioni con cui collabora le modalità in cui esse dovrebbero svolgere gli studi clinici sui loro candidati vaccini contro il COVID-19, stabilendo così una coordinazione operativa internazionale che permetta di valutare interventi globali che possano influenzare il corso della pandemia.
Come mai prima d’ora, le collaborazioni istituzionali sono necessarie: anche se, nel peggiore degli scenari, nessun vaccino contro il Covid-19 dovesse essere approvato, la velocizzazione delle fasi di ricerca e l’avviamento di filiere produttive parallele hanno reso il mondo più pronto ad affrontare future pandemie. Come ha detto Sir John Bell, Professore di medicina alla Oxford University: “Il rischio di nuove pandemie ci accompagnerà e i nuovi centri di ricerca renderanno il mondo più pronto e miglioreranno la nostra velocità di reazione la prossima volta che ci troveremo ad affrontare una tale sfida”.
------------
Clicca qui per conoscere gli ultimi aggiornamenti della WHO su tutti i potenziali vaccini contro il COVID-19.





Comments